Rompiendo la barrera bucal (3)
Jan 28, 2026
El descubrimiento, optimización y posterior modificación del PN-235 (icotrokinra, JN-2113)
Las ventajas de los péptidos cíclicos administrados por vía oral se han detallado en artículos anteriores, y el PN-235 recibe una atención significativa como uno de los pocos fármacos de péptidos cíclicos disponibles actualmente para administración oral. El 21 de julio de 2025, Protagonist y Janssen anunciaron que habían presentado una Solicitud de Nuevo Medicamento (NDA) a la FDA para Icotrokinra, para el tratamiento de la psoriasis en placas de moderada a grave en adultos y niños de 12 años o más. Si se aprueba, se espera que Icotrokinra se convierta en el primer fármaco oral del mundo dirigido al IL-23R para el tratamiento de la psoriasis. Este artículo se centra en el proceso de descubrimiento y las estrategias de optimización sistemática de esta molécula, utilizando las fechas de publicación de patentes como cronograma, y también resume las posibles direcciones para una mayor optimización.
Ya en 2007, Valorisation Hsj, Societe En Commandite presentó una solicitud de patente para antagonistas peptídicos IL-23R (WO2009007849). Esta es una de las primeras patentes sobre antagonistas peptídicos IL-23R en la información disponible públicamente. Esta patente describe una serie de péptidos dirigidos a IL-23R, incluido el agonista APG-2301 y los antagonistas APG-2303, APG-2305, APG-2307 y APG-2309 (las secuencias se muestran en la figura siguiente). El equipo utilizó la secuencia de aminoácidos de IL-23R como base, combinada con técnicas de modelado por computadora, para generar péptidos lineales correspondientes a su región bisagra (que imitan a IL-23 y actúan como antagonistas de IL-23R). Entre estos, APG-2305 y APG-2309 inhibieron eficazmente la fosforilación de STAT3 en esplenocitos de ratón in vitro, con valores de IC50 de 1 nM y 2 nM, respectivamente. Además, en un modelo de EII en ratas, el tratamiento con APG-2309 alivió significativamente el edema y el enrojecimiento inducidos por la inflamación y redujo significativamente la infiltración de leucocitos en la mucosa y la congestión vascular, lo que demuestra un buen potencial antiinflamatorio y terapéutico.

En 2013, Medical Diagnostic Laboratories (MDL) publicó una patente (US20130029907) que describe el descubrimiento de péptidos de unión a IL-23R-utilizando tecnología de presentación en fagos, identificando con éxito varias secuencias peptídicas que se unen específicamente a IL-23R. Esta investigación construyó una biblioteca de presentación en fagos M13 que contiene secuencias peptídicas aleatorias de 12-mer y realizó múltiples rondas de detección utilizando IL-23R recombinante soluble de longitud completa y sus variantes de empalme como objetivos. Finalmente, se identificaron 27 péptidos con actividad de unión. En particular, estas secuencias peptídicas mostraron una baja similitud con la estructura cristalina de IL-23 informada por Beyer et al. (ID del PDB: 3D85). Mediante la alineación de secuencias, los investigadores encontraron que el 66,7% de los péptidos contenían una secuencia de reconocimiento conservada: -WX1X2X3W-, que se planteó como motivo funcional clave para unirse a IL-23R y bloquear su transducción de señales posteriores (en la figura siguiente se muestra una secuencia representativa). Posteriormente, los investigadores evaluaron la actividad inhibidora de los péptidos sobre la unión de IL-23 a IL-23R mediante experimentos ELISA competitivos, identificando el péptido 23 (un péptido de 12 unidades) como el péptido más activo, que inhibió significativamente la unión de IL-23 a IL-23R (IC50=0.85 µM).

En base a esto, el equipo optimizó la estructura del péptido 23, incluida la extensión o acortamiento de los extremos C/N, la sustitución de aminoácidos internos por aminoácidos ácidos/neutrales/básicos y modificaciones de ciclación. Los resultados competitivos de ELISA mostraron que la extensión de aminoácidos en ambos extremos del péptido 23 tuvo poco efecto sobre su actividad inhibidora, pero el acortamiento condujo a una disminución de la actividad inhibidora. La modificación de las propiedades de carga de los residuos "X" en el motivo central -WX1X2X3W- (por ejemplo, reemplazar residuos cargados negativamente con otros residuos cargados negativamente, polares sin carga o cargados positivamente) no afectó significativamente su actividad inhibidora, lo que indica que las características de carga de los residuos en esta región no son determinantes clave de la actividad de unión. Reemplazar uno de los residuos de triptófano (W) en la estructura central con fenilalanina (F) o tirosina (Y) conservó su capacidad inhibidora, mientras que reemplazarlo con alanina (A) redujo la actividad, lo que es consistente con las características de secuencia obtenidas de exámenes de presentación de fagos anteriores.
Además, acortar el péptido 23.15 manteniendo la estructura central -WQDYW-, aunque se conservó el motivo central, debilitó significativamente su actividad inhibidora. Además, la introducción de cisteína (Cys) en ambos extremos para formar un péptido cíclico dio como resultado una actividad comparable a la del péptido lineal; sin embargo, reducir el tamaño del péptido cíclico a 7 o 9 péptidos manteniendo la estructura central debilitó significativamente su capacidad para inhibir IL-23R.

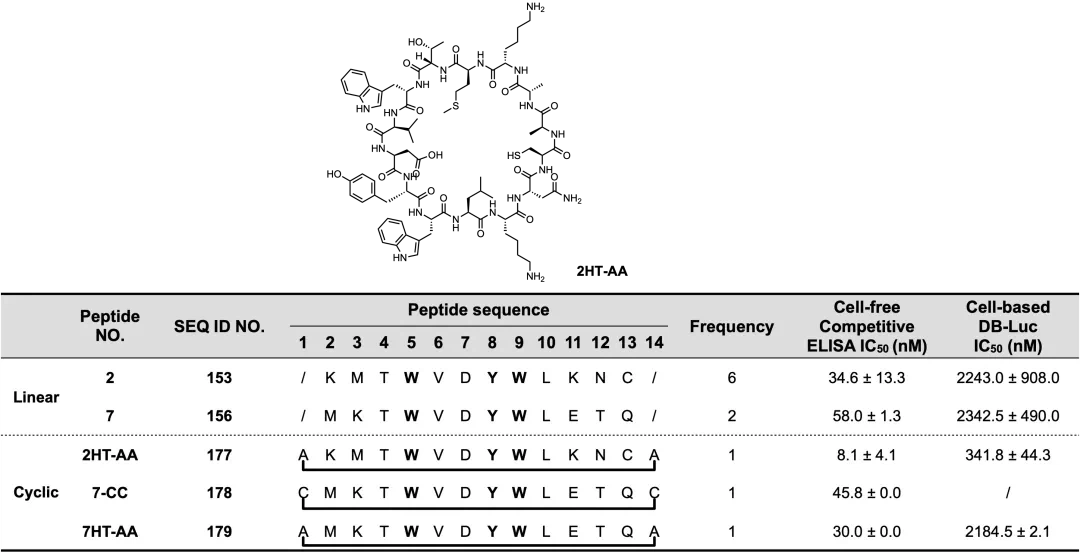
En dos patentes posteriores publicadas por MDL (US20130172272 y US20160039878), los investigadores utilizaron la estructura central -WX1X2X3W- como armazón y construyeron y examinaron una biblioteca de péptidos específicos utilizando tecnología de visualización de ribosomas (secuencia de la biblioteca de péptidos: XXXWXXYWXXXX). Después de ocho rondas de selección, los péptidos se subdividieron aún más según la estructura -WX1X2YW-: el grupo A contenía -WVDYW-, el grupo B contenía -WQDYW- y el grupo C contenía péptidos con otras secuencias centrales. Las pruebas de actividad ELISA mostraron que el Péptido No. 2/7 en el Grupo A tenía una actividad superior en comparación con el Péptido No. 23.19 divulgado en la patente anterior. En pruebas ELISA competitivas, el péptido No. 7 tenía una CI50 de 58,0 nM y el péptido No. 2 tenía una CI50 de 34,6 nM.

Posteriormente, utilizando el Péptido NO.2 y el Péptido NO.7 como puntos de partida, se diseñaron y sintetizaron tres péptidos cíclicos: 2HT-AA, 7-CC y 7HT-AA. Entre ellas, la molécula 2HT-AA, basada en la ciclación de cabeza-a-cola de residuos de alanina en ambos extremos del péptido NO.2, exhibió la mejor actividad (la estructura se muestra en la figura siguiente), con un ELISA IC50 competitivo de 8,1 nM y una actividad indicadora de 341,8 nM (método de prueba: IL-23 estimuló una célula DB línea transfectada con un gen indicador STAT3, y la actividad inhibidora se cuantificó detectando la expresión del gen indicador). Esto representó un aumento de 4-6 veces en la actividad en comparación con el péptido lineal. En pruebas de actividad in vitro, 2HT-AA inhibió eficazmente la secreción de IL-17F inducida por IL-23 en células Th17 humanas de una manera dependiente de la concentración y bloqueó la producción de IL-22 en PBMC humanas y esplenocitos de rata. Al mismo tiempo, este péptido cíclico también reguló negativamente los niveles de ARNm de IL-17F en esplenocitos de rata. Desafortunadamente, a pesar de la prometedora actividad farmacológica de 2HT-AA, no se han encontrado informes de optimización posteriores de esta estructura peptídica cíclica y sus derivados por parte de MDL.